| Autor |
Nachricht |
Chlorholiker
Gast
|
 Verfasst am: 27. Aug 2012 23:34 Titel: Chlor einatmen Verfasst am: 27. Aug 2012 23:34 Titel: Chlor einatmen |
 |
|
Meine Frage:
Hallo,
was passiert, wenn man Chlor einatmet, also was für eine Reaktion findet da statt?
Meine Ideen:
Halogene sind für uns Menschen sehr giftig, da sie oxidiernd wirken. Wenn man Chlor einatmet, dann könnten einige Stoffe in der Zelle oxidiert werden und dies würde vielleicht zu einer Fehlfunktion enzymatischer Abläufe führen.
Aber was wird denn oxidiert? |
|
 |
Firelion

Anmeldungsdatum: 27.08.2009
Beiträge: 1878
|
 Verfasst am: 27. Aug 2012 23:47 Titel: Verfasst am: 27. Aug 2012 23:47 Titel: |
 |
|
Hi,
soweit ich weiß ist Chlor ein Reizgas, dass die Atemwege angreift.
Reizgase sind in der Lage als unspezifische Reaktionen Entzündungen hervozurufen. Passiert das durch Inhalation in der Lunge, kann es dadurch zu einem Lungenödem kommen. Dadurch kann der Gasaustausch nicht mehr effizient erfolgen und der Tod durch Ersticken droht.
Ansonsten schätze ich mal das Chlor die Proteine oxidiert und damit das Gewebe zerstören kann.
LG Firelion
_________________
It is well known that a vital ingredient of success is not knowing that what youre attempting cant be done - Terry Pratchett |
|
 |
PaGe
Moderator

Anmeldungsdatum: 19.03.2007
Beiträge: 3549
Wohnort: Hannover
|
 Verfasst am: 27. Aug 2012 23:58 Titel: Verfasst am: 27. Aug 2012 23:58 Titel: |
 |
|
Chlor oxidiert wirklich so ziemlich alles. Daher nutzt(e) man es ja auch zum Bleichen. Und ohne vernünftige Zell- und Molekularstrukturen funktioniert die Sauerstoffaufnahme nicht mehr richtig.
Meines Wissens entsteht dabei auch Salzsäure. Wie viel Einfluss das dann allerdings noch hat, weiß ich nicht.
_________________
Die deutsche Rechtschreibung ist Freeware, du darfst sie kostenlos nutzen. Aber sie ist nicht Open Source, d. h., du darfst sie nicht verändern oder in veränderter Form veröffentlichen. |
|
 |
Chlorholiker
Gast
|
 Verfasst am: 28. Aug 2012 21:05 Titel: Verfasst am: 28. Aug 2012 21:05 Titel: |
 |
|
Hi,
danke für eure Antworten 
Also ich habe nochmal überlegt, und Chlor oxidiert ja so ziemlich alles...
Wenn ich nun eine Reaktionsgleichung angeben müsste, was passsiert, wenn man Cl2 einatmet, ist die hier richtig?
Cl2 + H2O reagiert zu : HCl + HOCl
In den Atemwegen sind doch auch bestimmt Wasser-Moleküle vorhanden, mit denen das Cl2 reagieren kann, oder?
Zusammengefasst:
Wenn nun die Raektion so stimmt, dann kan mann doch sagen, dass das Cl2 giftig ist, weil es stoffe oxidiert und dabei dann Salzsäure und Hypochlorige Säure entstehen, die dann weitere Zellbestandteile auflösen können. Dadurch funktionieren viele biologische Sachen nicht mehr. Außerdem kann Cl2 und/oder HCl + HOCl mit Proteinen bzw. Enzymen reagieren. Das würde doch zu einer Fehlfunktion enzymatischer Abläufe führen. |
|
 |
PaGe
Moderator

Anmeldungsdatum: 19.03.2007
Beiträge: 3549
Wohnort: Hannover
|
 Verfasst am: 28. Aug 2012 21:56 Titel: Verfasst am: 28. Aug 2012 21:56 Titel: |
 |
|
Chlor reagiert auch direkt mit den Strukturen. Dafür kann man nur keine Reaktionsgleichung angeben. Das Hypochlorid kann ähnlich dem Chlor reagieren. Daher verwendet man es auch in Badreinigern.
Die Reaktion mit Wasser ist aber prinzipiell richtig,
_________________
Die deutsche Rechtschreibung ist Freeware, du darfst sie kostenlos nutzen. Aber sie ist nicht Open Source, d. h., du darfst sie nicht verändern oder in veränderter Form veröffentlichen. |
|
 |
Hedera

Anmeldungsdatum: 08.03.2011
Beiträge: 657
|
 Verfasst am: 28. Aug 2012 22:21 Titel: Verfasst am: 28. Aug 2012 22:21 Titel: |
 |
|
Wenn Cl mit H2O unteranderem zu ClOH reagieren würde, dann hätte die Chemie ein großes Problem.
Wenn Chlor oder Chlorid (Cl-) mit Wasser reagieren, dann nur zu HCl, wobei das H positiv geladen und das Chlor negativ (daher Chlorid). Das Problem ist jetzt, dass Cl2 was das angeht total unreaktiv ist. Wenn du Cl-Gas in Wasser pumpen würdest, dann würde nur ein minimaler Teil mit dem Wasser reagieren. Das meiste würde einfachc ausströmen. Mit Chlorid sieht das anders aus. Wenn du Cl- ins Wasser schmeißt bildet sich munter HCl bzw. da wir uns in Wasser befinden sinkt der pH-Wert und wir haben mehr H+ (was die Cl- wieder ausgleicht).
Ich weiß selbst nicht, was Cl2 jetzt genau macht, aber wahrscheinlich wird es irgendeine Reaktion geben, woraus letztlich HCl entsteht. Da Cl ein Oxidationsmittel ist. Es wird möglicherweise mit Kohlenstoffmonoxid, Kohlensäure oder anderen reaktiven Stoffen reagierenund dann in einem zweiten Schritt zu HCl |
|
 |
jörg

Anmeldungsdatum: 12.12.2010
Beiträge: 2107
Wohnort: Bückeburg
|
 Verfasst am: 29. Aug 2012 00:42 Titel: Verfasst am: 29. Aug 2012 00:42 Titel: |
 |
|
slebstverständlich reagiert Chlor mit Wasser nicht nur unter Bildung von Salzsäure, sondern auch unter Bildung von hypochloriger Säure (HClO).
Die Chemie hat damit kein Problem:
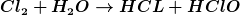
Auch wenn die Rückreaktion zu Chlorwasser energetisch günstiger ist, so entsteht doch hypochlorige Säure (u.a. weil die Salzsäure dem Gleichgewicht entzogen wird) bei Einatmung von Chlorgasen aufgrund der Feuchtigkeit im Atemtrakt und hat Anteil an der Toxizität.
_________________
RNA?- just another nucleic acid? |
|
 |
Hedera

Anmeldungsdatum: 08.03.2011
Beiträge: 657
|
 Verfasst am: 29. Aug 2012 11:20 Titel: Verfasst am: 29. Aug 2012 11:20 Titel: |
 |
|
Das würde bedeuten, dass bei der Chlorgasspaltung Cl+ und Cl- entsteht. Wie soll das bitte gehen? Das Funktioniert auf dem Papier aber sonst nicht. Die Elektronegativität blockiert dir das. Damit du das schaffst brauchst du irgendeine weitere Vor-Rekation. In diesem Fall ist es dann kein Problem, aber deine Reaktionsgleichung, wie sie da steht ist nicht korrekt.
Es würde mich ziemlich wundern, wenn das geht. Aber ich lasse mich auch eines besseren belehren, wenn du ne Quelle hast  |
|
 |
jörg

Anmeldungsdatum: 12.12.2010
Beiträge: 2107
Wohnort: Bückeburg
|
|
 |
Hedera

Anmeldungsdatum: 08.03.2011
Beiträge: 657
|
 Verfasst am: 29. Aug 2012 12:26 Titel: Verfasst am: 29. Aug 2012 12:26 Titel: |
 |
|
Mein Problem war, dass du beim Spalten von Cl2 ja Cl+ und Cl- bekommen musst, was aber bei einer gleichwertigen EN von Cl nicht ohne weiteres passiert. Und genau das wird ja durch das Gleichgewicht auch gezeigt. Ich persönlich tendiere daher auch eher dazu, dass Cl2 + H+ zu HCl + Cl+ reagiert und dann das Cl+ weiter zu ClOH. Das müsste man mal experimentell untersuchen. Meiner Meinung nach dürfte eben im basischen Bereicht garnichts passieren und im saurem viel HCl und nahe zu garkein ClOH.
Aber wie schon gesagt so gut kenn ich mich damit auch nicht aus  |
|
 |
PaGe
Moderator

Anmeldungsdatum: 19.03.2007
Beiträge: 3549
Wohnort: Hannover
|
 Verfasst am: 29. Aug 2012 16:58 Titel: Verfasst am: 29. Aug 2012 16:58 Titel: |
 |
|
Es entsteht kein Cl+, sondern ein OCl-.
Aber wie jörg und ich schon geschrieben haben. Die Reaktion ist nicht unbedingt begünstigt und hat ein Gleichgewicht auf der Seite des Chlorwassers. Sie ist aber prinzipiell möglich.
Ich weiß allerdings nicht, ob man es mit einfachen Mitteln experimentell überprüfen kann. Indikatoren fallen ja weg, da sie oxidiert werden. Und selbst mit einer pH-Sonde stelle ich mir es schwer vor. Und dann ist Chlor ja auch noch so schlecht wasserlöslich.
_________________
Die deutsche Rechtschreibung ist Freeware, du darfst sie kostenlos nutzen. Aber sie ist nicht Open Source, d. h., du darfst sie nicht verändern oder in veränderter Form veröffentlichen. |
|
 |
Hedera

Anmeldungsdatum: 08.03.2011
Beiträge: 657
|
 Verfasst am: 29. Aug 2012 18:40 Titel: Verfasst am: 29. Aug 2012 18:40 Titel: |
 |
|
Da sehe ich aber das Problem beim Sauersoff. Woher soll der denn bitte kommen?
Und das lässt sich experimentell durchaus untersuchen, wobei das natürlich keine Knallgasprobe sein wird  |
|
 |
PaGe
Moderator

Anmeldungsdatum: 19.03.2007
Beiträge: 3549
Wohnort: Hannover
|
 Verfasst am: 29. Aug 2012 22:26 Titel: Verfasst am: 29. Aug 2012 22:26 Titel: |
 |
|
Wasser ist H2O, daher muss er kommen. Das hat doch jörg schon geschrieben. Knallgasprobe ist was völlig anderes. Ds Problem ist, dass es ein Nachweis sein muss, der unempfindlich gegenüber Oxidation sein muss. Das ist die Schwierigkeit.
_________________
Die deutsche Rechtschreibung ist Freeware, du darfst sie kostenlos nutzen. Aber sie ist nicht Open Source, d. h., du darfst sie nicht verändern oder in veränderter Form veröffentlichen. |
|
 |
Hedera

Anmeldungsdatum: 08.03.2011
Beiträge: 657
|
 Verfasst am: 30. Aug 2012 13:08 Titel: Verfasst am: 30. Aug 2012 13:08 Titel: |
 |
|
Ja und genau das ist mein Problem. Du kannst nicht einfach ohne weiteres H2O oder OH spalten. Woher soll die Energie kommen?
Und das mit der Knallgasprobe war ein: "Natürlich wird es komplizierter als eine Reaktion in der Wasserstoff freigesetzt wird zu untersuchen ---> Knallgasprobe"
Das hatte keinerlei inhaltlichen Zusammenhang  |
|
 |
jörg

Anmeldungsdatum: 12.12.2010
Beiträge: 2107
Wohnort: Bückeburg
|
 Verfasst am: 30. Aug 2012 16:28 Titel: Verfasst am: 30. Aug 2012 16:28 Titel: |
 |
|
Wasser dissoziiert spontan, zumindest etwas. In H2O hast du also auch immer einen Anteil H+ sowie OH-. Entziehst du diese jetzt dem Gleichgewicht, z.B. durch Reaktion mit irgendwas, dann dissoziiert natürlich Wasser nach, da H2O ja mit H+ und OH- im Gleichgewicht steht und nicht mit irgendwas.
Ehrlich gesagt verstehe ich dein Problem überhaupt nicht, denn wenn man weiss, dass Chlor die Oxidationszahlen von -1 bis +7 einnehmen kann, sieht man, dass die Entstehung von HClO (hier hat Chlor die Oxidationszahl +1, Sauerstoff -2 und Wasserstoff +1) genausowenig verwunderlich ist wie die Entstehung der anderen sauerstoffhaltigen Säuren des Chlor, in denen Chlor noch höhere Oxidationszahlen hat (bei HClO4 dann +7).
_________________
RNA?- just another nucleic acid? |
|
 |
PaGe
Moderator

Anmeldungsdatum: 19.03.2007
Beiträge: 3549
Wohnort: Hannover
|
 Verfasst am: 30. Aug 2012 18:43 Titel: Verfasst am: 30. Aug 2012 18:43 Titel: |
 |
|

_________________
Die deutsche Rechtschreibung ist Freeware, du darfst sie kostenlos nutzen. Aber sie ist nicht Open Source, d. h., du darfst sie nicht verändern oder in veränderter Form veröffentlichen. |
|
 |
Hedera

Anmeldungsdatum: 08.03.2011
Beiträge: 657
|
 Verfasst am: 03. Sep 2012 16:37 Titel: Verfasst am: 03. Sep 2012 16:37 Titel: |
 |
|
Das Problem ist folgendes:
| Zitat: | | Es entsteht kein Cl+, sondern ein OCl- |
| Zitat: | | Wasser ist H2O, daher muss er kommen |
Ihr müsst mir hier keine Basics der Säure-Basen-Chemie erklären. Aber das was ihr mir hier verkaufen wollt hat nichts damit zu tun.
Es steht einfach kein Sauerstoff zur Reaktion zur verfügung, sondern nur H2O, H+ und OH-.
Und selbst verständlich kann Cl die Oxidationsstufen einnehmen. Aber auch hier müssen dir richtigen Bedinungen vorhanden sein. Und nur weil etwas formal geht heißt das noch lange nicht, dass dem wirklich so ist und vorallem ist ganz entscheiden ob überhaupt genug Energie vorhanden ist. |
|
 |
PaGe
Moderator

Anmeldungsdatum: 19.03.2007
Beiträge: 3549
Wohnort: Hannover
|
 Verfasst am: 03. Sep 2012 16:49 Titel: Verfasst am: 03. Sep 2012 16:49 Titel: |
 |
|
| Zitat: | | Es steht einfach kein Sauerstoff zur Reaktion zur verfügung, sondern nur H2O, H+ und OH-. |
Wofür brauchst du denn den Sauerstoff? Das ganze läuft auch ohne Sauerstoff ab. Oxidation muss doch keine Reaktion mit Sauerstoff sein.
Und dass die Reaktion, wenn auch in sehr geringem Ausmaß, steht bei Wiki mit einer Quelle. Ich habe das Nich nicht hier, aber da könntest du nachschauen.
http://en.wikipedia.org/wiki/Hypochlorous_acid
Und da das Entfernen der Salzsäure durch Quecksilberoxid (deutsche Wiki) ist auch nur eine Gleichgewichtsverschiebung, sodass die Reaktion schon vorher möglich gewesen sein muss.
_________________
Die deutsche Rechtschreibung ist Freeware, du darfst sie kostenlos nutzen. Aber sie ist nicht Open Source, d. h., du darfst sie nicht verändern oder in veränderter Form veröffentlichen. |
|
 |
Daniel35
Gast
|
 Verfasst am: 03. Sep 2012 22:36 Titel: Verfasst am: 03. Sep 2012 22:36 Titel: |
 |
|
| Hedera hat Folgendes geschrieben: | Das Problem ist folgendes:
Ihr müsst mir hier keine Basics der Säure-Basen-Chemie erklären. Aber das was ihr mir hier verkaufen wollt hat nichts damit zu tun.
Es steht einfach kein Sauerstoff zur Reaktion zur verfügung, sondern nur H2O, H+ und OH-.
|
OH- reicht doch auch vollkommen.
Betrachte es als nukleophile Substitution mit Cl- als Abgangsgruppe.
Die hypochlorige Säure wird dann natürlich deprotoniert. |
|
 |
Hedera

Anmeldungsdatum: 08.03.2011
Beiträge: 657
|
 Verfasst am: 04. Sep 2012 13:55 Titel: Verfasst am: 04. Sep 2012 13:55 Titel: |
 |
|
Ja, wir haben offensichtlich an einander vorbei geredet.
| Zitat: | | Es entsteht kein Cl+, sondern ein OCl-. |
Diese Aussage ist nicht ganz korrekt. Es entsteht sehr wohl ein Cl+, was dann aber mit OH- reagiert und über ClOH zu OCl- dissoziert.
Das GGW liegt aber so extrem auf H2O + Cl2, als das ich beim Einatmen von Cl2 diese Reaktion nicht annehmen würde. Wobei das vielleicht natürlich auch mit den Druckbedingungen und so ganz anders aussehen kann. |
|
 |
Daniel35
Gast
|
 Verfasst am: 04. Sep 2012 15:32 Titel: Verfasst am: 04. Sep 2012 15:32 Titel: |
 |
|
|
Da "entsteht" sicher kein freies Chloronium-Ion. |
|
 |
Hedera

Anmeldungsdatum: 08.03.2011
Beiträge: 657
|
 Verfasst am: 04. Sep 2012 15:53 Titel: Verfasst am: 04. Sep 2012 15:53 Titel: |
 |
|
Formal  |
|
 |
Daniel35
Gast
|
 Verfasst am: 04. Sep 2012 16:23 Titel: Verfasst am: 04. Sep 2012 16:23 Titel: |
 |
|
OK, deine Argumente schienen mir aber nicht auf formale Reaktionsgleichungen sondern auf konkreten mechanistischen Argumenten zu beruhen.
Formal ist H2O der Sauerstofflieferant |
|
 |
PaGe
Moderator

Anmeldungsdatum: 19.03.2007
Beiträge: 3549
Wohnort: Hannover
|
 Verfasst am: 04. Sep 2012 17:25 Titel: Verfasst am: 04. Sep 2012 17:25 Titel: |
 |
|
Ob da ein Chloronium-Ion entsteht, bezweifel ich zwar. Ich denke, dass das ein bimolekularer Mechanismus ist.
Allerdings diskutieren wir hier wirklich Sachen, die kaum Relevanz für das Einatmen von Chlor hat.

_________________
Die deutsche Rechtschreibung ist Freeware, du darfst sie kostenlos nutzen. Aber sie ist nicht Open Source, d. h., du darfst sie nicht verändern oder in veränderter Form veröffentlichen. |
|
 |
jörg

Anmeldungsdatum: 12.12.2010
Beiträge: 2107
Wohnort: Bückeburg
|
 Verfasst am: 06. Sep 2012 19:19 Titel: Verfasst am: 06. Sep 2012 19:19 Titel: |
 |
|
| Hedera hat Folgendes geschrieben: | | Das GGW liegt aber so extrem auf H2O + Cl2, als das ich beim Einatmen von Cl2 diese Reaktion nicht annehmen würde. Wobei das vielleicht natürlich auch mit den Druckbedingungen und so ganz anders aussehen kann. |
Das mit dem Gleichgewicht stimmt - in wässriger Lösung, in dem dem HCl keine weiteren Reaktionspartner zur Verfügung stehen. Das ist aber im Gewebe anders, hier stehen dem HCl mehr als genug Reaktionspartner zur Verfügung, so dass zunehmend und recht schnell HCl aus dem Gleichgewicht entfernt wird. Also brauchst du keine besonderen Druckbedingungen o.ä., sondern musst -wie bei der Herstellung von Bleichungsmitteln (zumindest haben wir das in der Schule so gemacht), lediglich HCl aus dem Gleichgewicht entfernen.
Hypochlorige Säure/Hypochlorid hat dabei Anteil an der Toxizität von Chlorgasen.
| Daniel35 hat Folgendes geschrieben: | | OK, deine Argumente schienen mir aber nicht auf formale Reaktionsgleichungen sondern auf konkreten mechanistischen Argumenten zu beruhen. |
Das war auch mal so:
| Hedera hat Folgendes geschrieben: | | Und nur weil etwas formal geht heißt das noch lange nicht, dass dem wirklich so ist |
Auch wenn PaGe recht hat, noch eine Frage:
@Daniel35: Gibt es wirklich freie Chloronium-Ionen?
Bin da auf folgenden Artikel gestossen:
http://pubs.acs.org/doi/pdf/10.1021/ol070673n
Zu dem Journal habe ich aber leider keinen Zugriff und aus dem abstract geht für mich nicht eindeutig hervor, ob es freie Cl+-Ionen gibt. Formal gesehen - o.k., aber können die frei nachgewiesen werden oder kommen die "nur" intermediär vor?
_________________
RNA?- just another nucleic acid? |
|
 |
PaGe
Moderator

Anmeldungsdatum: 19.03.2007
Beiträge: 3549
Wohnort: Hannover
|
 Verfasst am: 06. Sep 2012 19:40 Titel: Verfasst am: 06. Sep 2012 19:40 Titel: |
 |
|
Ich habe zwar auch keinen Zugriff, aber dabei geht es um Carbenium-Ionen (C+), an denen ein Chloratom hängt. Wenn ich die Zeichnung richtig intepretiere, geht es in dem Artikel darum, ob das Halogenatom (gleichzeitig) zwei Einfachbindungen zu den Kohlenstoffatomen ausbildet (und damit eine positive Partialladung tragen würde) oder wechselnde Einfachbindungen eingeht.
_________________
Die deutsche Rechtschreibung ist Freeware, du darfst sie kostenlos nutzen. Aber sie ist nicht Open Source, d. h., du darfst sie nicht verändern oder in veränderter Form veröffentlichen. |
|
 |
|